La prise en charge des patients atteints de sclérose latérale amyotrophique (SLA) requiert une approche holistique multidisciplinaire spécialisée.
Les traitements pharmacologiques modificateurs de la maladie pour la SLA incluent le riluzole et l’édaravone.
Il faut porter une grande attention au soutien nutritionnel et aux soins respiratoires pour une prise en charge optimale de la SLA.
Plusieurs traitements sont disponibles pour alléger les symptômes de la SLA.
Les soins palliatifs et le soutien aux proches aidants sont d’importants éléments pour accompagner les patients durant leur cheminement les confrontant à la SLA.
La sclérose latérale amyotrophique (SLA) est une maladie progressive invalidante due à une dégénérescence des motoneurones dans le cerveau et la moelle épinière; elle provoque faiblesse, atrophie musculaire, fasciculations et spasticité1. La forme la plus fréquente est une faiblesse qui affecte d’abord les membres, suivie de problèmes de mobilité chez près de 70 % des patients2. La forme bulbaire, accompagnée d’une atteinte des muscles oropharyngés nuisant à la déglutition et au langage, s’observe dans environ 25 % des cas2. En plus de l’atteinte motrice, une dégénérescence au niveau des lobes frontaux et temporaux qui entraîne une atteinte cognitive ou comportementale, s’observe chez jusqu’à 50 % des patients3. Avec le temps, la force diminue, et les patients décèdent en général d’insuffisance respiratoire dans les 5 ans qui suivent le diagnostic2. Malgré l’intensification de la recherche ces dernières années, les options thérapeutiques pour la SLA demeurent limitées et les soins aux patients concernent principalement le soulagement des symptômes et une optimisation du fonctionnement et de la qualité de vie2.
On estime à 3000 le nombre de Canadiennes et de Canadiens actuellement aux prises avec la SLA4,5. Des groupes de défense des intérêts et des médecins qui soignent ces patients se sont mobilisés pour obtenir des recommandations sur les soins et la prise en charge optimale de ces patients au Canada. Des lignes directrices de pratique clinique sur la SLA ont été publiées aux États-Unis6,7 et en Europe8,9, mais à ce jour, aucune n’a porté spécifiquement sur les soins aux patients atteints de SLA au Canada.
En plus de fournir une mise à jour sur les normes thérapeutiques en constante évolution pour la SLA, les pratiques optimales recommandées dans cette ligne directrice permettent d’aborder plusieurs enjeux importants pour la population canadienne, tels que le soutien aux proches aidants, la gestion de la pharmacothérapie et l’aide médicale à mourir (AMM). La rédaction d’une première ligne directrice canadienne sur la SLA constitue une étape cruciale dans un processus qui permettra d’actualiser ces recommandations à mesure que de nouvelles données probantes se feront jour; sans compter qu’elle permettra d’identifier et de prioriser les sujets abordés par la recherche et de combler les lacunes sur le plan des connaissances.
Étant donné que la rigueur généralement attendue des recommandations médicales fondées sur des données probantes est difficile à observer pour ce qui est des différents aspects du traitement de la SLA, plusieurs des recommandations présentées ici reposent sur le consensus des experts relativement aux bonnes pratiques. En général, la prise en charge des symptômes de la SLA s’inspire des données probantes générées pour d’autres pathologies. Les recommandations de cette ligne directrice se fondent sur les meilleures données probantes disponibles et sur le consensus des experts quant aux pratiques optimales, et sont donc le reflet de l’expérience pratique des médecins canadiens qui soignent des patients atteints de la SLA. Cet article est un sommaire de la ligne directrice intégrale, que l’on peut consulter sur le site Web de la Société canadienne de la SLA, à l’adresse (www.als.ca/bpr-appendix).
Portée
Le but de cette ligne directrice est d’offrir aux médecins, aux autres professionnels de la santé et aux omnipraticiens qui soignent des personnes atteintes de la SLA des recommandations de pratiques optimales pour les soins et la prise en charge des patients vivant avec la SLA, sans égard aux questions de sexe, de genre, d’âge ou au stade de la maladie. Cette ligne directrice devrait mener à l’élaboration d’une norme nationale afin d’améliorer la qualité des soins, au bénéfice des patients, des familles et des proches aidants affectés par la SLA. Les groupes de défense (p. ex., la Société canadienne de la SLA et ses sections provinciales), les instances sanitaires, les gouvernements et les responsables des orientations politiques seront ainsi mieux à même d’établir des normes de soins et d’en faire la promotion.
Recommandations
Les soins et la prise en charge des patients atteints de SLA devraient toujours être centrés sur les patients, sans négliger les dimensions holistiques et émotionnelles de leur bien-être. C’est au patient qu’il revient de décider de son traitement, ce qui inclut l’option d’abaisser le niveau d’intervention.
Les recommandations pour la prise en charge des patients atteints de SLA au Canada se trouvent au tableau 1, regroupées par thème, avec le niveau des données probantes. Si les données probantes étaient insuffisantes ou absentes pour une question clé, nous avons formulé des recommandations fondées sur le consensus des experts après examen de la littérature disponible et de l’expérience clinique en matière de SLA, ou sur l’extrapolation des traitements prodigués pour d’autres maladies plus communes.
Recommandations assorties du niveau de données probantes pour la prise en charge des patients atteints de sclérose latérale amyotrophique*
Les sections suivantes fournissent un contexte et expliquent certaines recommandations reposant sur des données probantes. Le tableau des données probantes, à l’annexe C de la ligne directrice intégrale (accessible ici www.als.ca/bpr-appendix), fournit des détails sur les données probantes à l’appui de toutes les recommandations présentées au tableau 1. Pour une explication complète des données probantes à l’appui des recommandations, veuillez consulter l’annexe A (www.als.ca/bpr-appendix).
Annonce du diagnostic
La façon d’annoncer le diagnostic de SLA est source de mécontentement chez plusieurs patients et proches aidants10,11. Des recommandations générales ont été formulées sur la façon d’annoncer le diagnostic de SLA8. Les médecins devraient principalement s’adapter aux besoins de chaque patient. Si un patient est incapable d’absorber la nouvelle du diagnostic de SLA, il peut être préférable d’y aller par étapes, sans tout dévoiler à la fois12. À l’inverse, d’autres patients peuvent avoir l’impression d’avoir trop peu d’informations lors du diagnostic; les patients et les proches aidants souhaitent parfois qu’on les renseigne sur l’état de la recherche, des traitements et du pronostic au moment du diagnostic13.
Dans une étude sur la satisfaction quant à la façon d’annoncer le diagnostic de SLA, 41 % des patients ont indiqué avoir reçu des renseignements insuffisants, et un tiers a précisé ne pas avoir eu les coordonnées d’une personne-ressource auprès de qui faire un suivi10. En outre, environ 75 % des patients et des proches aidants avaient des questions immédiatement après l’annonce du diagnostic11. Ces observations rappellent qu’après l’annonce du diagnostic, les médecins doivent proposer des sources d’information, fournir les coordonnées de ressources communautaires et offrir un suivi rapide. Les patients se disent plus satisfaits de l’annonce du diagnostic de SLA s’ils croient que le médecin a compris ce qu’ils ressentent13. Une source additionnelle de frustration pour les patients a été le retard de confirmation du diagnostic, y compris le temps d’attente pour voir un spécialiste de la SLA10. Le groupe de travail a fixé à 4 semaines le délai maximal raisonnable pour obtenir une consultation de confirmation d’un diagnostic de SLA.
Traitement modificateur de la maladie
En 2000, Santé Canada a approuvé le riluzole pour le traitement de la SLA. Selon une méta-analyse de classe I regroupant 4 essais randomisés et contrôlés (ERC), le riluzole offre un avantage modeste sur la survie comparativement au placebo, avec un rapport de risque (HR) de 0,84 (intervalle de confiance [IC] de 95 % 0,698 à 0,997), représentant un gain de 9 % de la probabilité de survie annuelle. Cela se traduit par une augmentation médiane de la survie de 11,8 à 14,8 mois14. De récentes études de cohorte (toutes de classe III) basées sur un registre ont estimé l’amélioration de la survie médiane avec le traitement par riluzole à 7,3 mois15, 10 mois16 ou 12 mois17, tandis que d’autres études n’ont fait état d’aucun effet sur la survie18–21. Les résultats d’autres études de cohorte de classe III ont donné des estimations du HR de 0,3422, 0,7123, 0,7924 et 0,8125, ce qui se traduit par une augmentation absolue de la survie annuelle estimée allant de 10 % à 50 %.
Aucun essai contrôlé n’a vérifié si le riluzole prolonge la vie à un stade spécifique ou à tous les stades de la SLA. Selon une analyse post hoc de l’étude originale d’établissement des doses, le riluzole pourrait être efficace à prolonger la survie uniquement aux stades plus avancés de la maladie (définis par une détérioration nutritionnelle ou respiratoire suffisante pour nécessiter une intervention)26, mais les résultats d’autres études de cohorte diffèrent, montrant qu’il pourrait être efficace uniquement lors des stades moins avancés27 ou que son effet sur la survie est de courte durée28. Néanmoins, des décennies d’expérience à l’échelle mondiale ont montré que le riluzole est en général bien toléré lors d’une utilisation prolongée et moyennant une surveillance régulière des enzymes hépatiques et des numérations sanguines, des nausées et de la fatigue (classe I)14.
En octobre 2018, Santé Canada a approuvé l’édaravone pour traiter la SLA. Une seule étude de classe 1 dans une population généralisée souffrant de SLA a échoué à démontrer un bienfait général de l’édaravone sur le ralentissement de la progression du score ALSFRS-R (ALS functional rating scale – revised) sur une période de 6 mois29, mais a évoqué un avantage chez un sousgroupe de patients (voir tableau 1 pour les caractéristiques de ce sous-groupe). Cet effet bénéfique sur le ralentissement de la progression du score ALSFRS-R a par la suite été confirmé par une deuxième étude de classe 1 qui restreignait le recrutement aux patients présentant les caractéristiques du sous-groupe de la première étude30. La seconde étude a démontré une réduction moyenne du changement du score ALSFRS-R sur une période de 6 mois de 2,49 (IC de 95 % 0,99 à 3,98). Pour l’instant, les données probantes disponibles laissent entendre des données probantes de niveau B, « probablement efficace » chez un groupe sélectionné de patients atteints de SLA.
Multidisciplinarité des soins
Les patients atteints de SLA devraient être suivis régulièrement dans une clinique multidisciplinaire de SLA de concert avec leurs médecins traitants. Les soins multidisciplinaires devraient être prodigués par une équipe composée de médecins et d’autres professionnels de la santé chargés de veiller à divers paramètres, notamment communication, nutrition, déglutition, mobilité, activités de la vie quotidienne, soins respiratoires, capacité cognitive, enjeux psychosociaux, traitements médicaux et soins de fin de vie. Chez les patients suivis dans une clinique multidisciplinaire on a enregistré de meilleurs résultats, y compris amélioration de la survie, réduction des hospitalisations, utilisation accrue d’équipements adaptés et meilleure qualité de vie, comparativement aux patients qui n’étaient pas suivis dans ce type de clinique31–33. Selon une étude de cohorte prospective, les patients suivis dans une clinique multidisciplinaire vivaient 7,5 mois de plus que les patients suivis dans une clinique de neurologie générale32.
La télémédecine et la surveillance à distance sont faisables et pourraient compléter les soins multidisciplinaires en clinique34. La prise en charge des patients atteints de SLA devrait être une collaboration entre le médecin de famille et la clinique de SLA, le personnel de cette dernière se montrant disponible pour des consultations à distance entre les visites des patients.
Soins respiratoires
Le groupe responsable des lignes directrices émises par la Société canadienne de thoracologie (SCT) a récemment révisé la prise en charge respiratoire des patients atteints de SLA sous ventilation mécanique à domicile35. Nous avons décidé de faire concorder nos recommandations sur la prise en charge respiratoire (tableau 1, figure 1) avec celles de la SCT. Nous y avons cependant fait quelques ajouts, notamment un énoncé sur l’évitement de l’oxygénothérapie pour les symptômes respiratoires chez les patients atteints de SLA, le moment de l’instauration des interventions et la gestion des sécrétions. Nous avons aussi jugé important d’ajuster le critère de capacité vitale forcée (CVF) minimale pour l’instauration de la ventilation non effractive chez les patients asymptomatiques à 65 % des valeurs prévues, par rapport à la recommandation de la SCT (50 %), en raison des données probantes existantes selon lesquelles l’instauration précoce améliore la survie36. Les patients qui ont une CVF supérieure à 65 % de la valeur prévue peuvent débuter une ventilation non effractive si tout autre critère à cet effet est présent, conformément aux lignes directrices de la SCT. Notre groupe a aussi unanimement jugé que si les critères d’instauration de la ventilation non effractive sont présents, il faudrait la débuter dans les 4 semaines.
Arbre décisionnel respiratoire : Sommaire des recommandations pour les soins respiratoires chez les patients atteints de sclérose latérale amyotrophique (SLA), y compris ventilation (A) et clairance des voies respiratoires (B). Remarque : CVF = capacité vitale forcée, CVL = capacité vitale lente, DPT = débit de pointe à la toux, H2O = eau, IEM = insufflation–exsufflation mécanique, pCO2 = pression partielle du gaz carbonique, PIM = pression respiratoire maximale, PIN = pression inspiratoire nasale, RVP = recrutement de volume pulmonaire, VNE = ventilation non effractive.
Il est important de reconnaître que la ventilation non effractive peut modifier la trajectoire naturelle de la maladie. Par exemple, une dépendance accrue à l’endroit de la ventilation non effractive transforme cette dernière en une intervention de maintien des fonctions vitales. En effet, chez les patients dépendants de la ventilation non effractive, cette dernière prévient la mort naturelle aussi longtemps qu’une décision n’est pas délibérément prise de cesser la ventilation. Les patients devraient être informés qu’ils pourraient devoir prendre une décision délibérée au sujet de l’arrêt éventuel de la ventilation, à moins de vouloir prolonger leur survie.
La gestion des sécrétions est souvent difficile chez les personnes atteintes de SLA, et c’est une cause de détresse, de réduction de la qualité de vie et de dysfonction respiratoire. Les lignes directrices de la SCT ne mentionnent pas explicitement la clairance des voies respiratoires. Pour aborder cet important enjeu, nous avons passé en revue les données probantes disponibles et l’expérience clinique. Nous recommandons des techniques de récupération du volume respiratoire dès que les patients ont des sécrétions encombrantes ou présentent des difficultés à éliminer les sécrétions. Ces techniques peuvent être combinées avec des techniques manuelles d’assistance à la toux et effectuées par les patients seuls ou avec l’aide de professionnels de la santé. Si les patients présentent un débit de pointe à la toux (DPT) anormal (< 270 L/min), l’insufflation–exsufflation mécanique biquotidienne est à envisager pour éliminer les sécrétions, et plus fréquemment lors d’infections respiratoires aiguës.
Nous convenons aussi qu’il est essentiel de fournir un soutien respiratoire adéquat là où réside le patient avec la ventilation non effractive et l’insufflation–exsufflation mécanique à des fins d’enseignement, de titrage et de résolution de problèmes, indépendamment du lieu de résidence du patient (domicile, établissement de soins de longue durée ou centre de soins palliatifs).
Nutrition
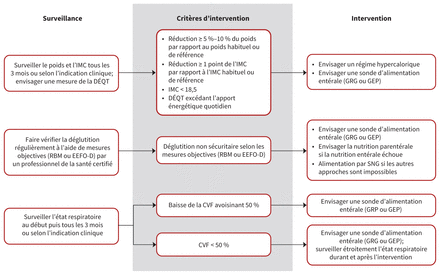
Les recommandations nutritionnelles (tableau 1, figure 2) suivent passablement celles que l’on retrouve dans la ligne directrice de l’American Academy of Neurology (AAN)6. Les différences par rapport aux recommandations de l’AAN incluent l’ajout de l’énoncé du consensus des experts sur le délai maximum de 4 semaines envisageable avant la pose d’une sonde d’alimentation une fois les critères présents, et d’un énoncé concernant le suivi approprié après l’insertion pour prévenir les complications immédiates ou tardives. Les recommandations incluent aussi un énoncé sur la composition de l’alimentation et précisent que des régimes hypercaloriques peuvent être utilisés pour améliorer les indicateurs nutritionnels et possiblement la survie37,38. Les régimes hypercaloriques–hyperglucidiques pourraient être préférables aux régimes hypercaloriques–hyperlipidiques39.
Arbre décisionnel nutritionnel : Sommaire des recommandations pour la prise en charge nutritionnelle des patients atteints de sclérose latérale amyotrophique (SLA). Remarque : CVF = capacité vitale forcée, DÉQT = dépense énergétique quotidienne totale, EEFO-D = évaluation endoscopique par fibre optique de la déglutition, GEP = gastrostomie endoscopique percutanée, GRG = gastrostomie radioguidée, IMC = indice de masse corporelle, RBM = repas baryté modifié, SNG = sonde nasogastrique.
Thromboembolie veineuse
Les patients atteints de SLA40,41 sont probablement exposés à un risque plus grand de thromboembolie veineuse (TEV). Le risque semble aggravé lorsque la SLA affecte d’abord les membres inférieurs et que la mobilité diminue40. Malgré ce risque accru, aucune étude n’appuie le recours à la thromboprophylaxie primaire. Pour l’instant, cette dernière n’est pas recommandée parce qu’on ignore le rapport risque–bénéfice des conséquences potentiellement négatives d’une chute par rapport à la prévention de la TEV chez les patients atteints de SLA.
Gestion de la pharmacothérapie
Lorsque les patients consultent dans une clinique de SLA, ils prennent souvent plusieurs médicaments qui ne sont peutêtre pas tous indispensables, particulièrement si l’on tient compte de la survie moyenne des patients atteints de SLA. Selon le consensus des experts, nous avons rédigé plusieurs énoncés sur l’importance de réviser régulièrement les médicaments du patient et de suggérer l’arrêt de tout agent non essentiel, qui ne soulage pas ses symptômes ou ne lui procure aucun bienfait thérapeutique approprié compte tenu de son espérance de vie.
Soulagement des symptômes
Les patients atteints de SLA ont souvent plusieurs types de symptômes incommodants qui nuisent gravement à leur qualité de vie, notamment douleur, fasciculations, sialorrhée, syndrome pseudobulbaire, spasticité, crampes, dépression, anxiété, insomnie et fatigue. Plusieurs essais cliniques ont exploré le traitement de la sialorrhée42 et du syndrome pseudobulbaire43. Toutefois, la prise en charge de la plupart des symptômes de la SLA n’a pas été rigoureusement évaluée. C’est pourquoi la majeure partie des recommandations pour la prise en charge des symptômes ont été établies par un consensus d’expert et s’appuient sur des suggestions formulées dans la littérature sur la SLA et les soins palliatifs. Le coût des traitements et leur accessibilité ont influencé le classement de nos recommandations et nous avons accordé plus de poids à ces 2 critères qu’aux données probantes directes si un traitement reposant sur des données probantes était coûteux. Nos recommandations n’ont pas inclus le cannabis pour le traitement de symptômes spécifiques de la SLA, en raison de l’absence de données probantes dans la littérature. Mais le groupe de travail sait que le cannabis est utilisé pour gérer plusieurs des symptômes de la SLA.
Dysarthrie
La capacité d’exprimer ses idées et ses besoins est vitale pour tous. La SLA nuit souvent à la capacité de communiquer verbalement en raison de la dysarthrie2. Il existe des outils non technologiques pour faciliter la communication, dont les tableaux de lettres ou de pictogrammes, et des outils technologiques, tels que les synthétiseurs vocaux et les systèmes à commande oculaire. À mesure que les pertes fonctionnelles se manifestent chez la personne atteinte de SLA, certains modes de communication pourraient ne plus être adaptés. Fournir l’accès à différents modes de communication, y compris les médias sociaux, peut préserver l’autonomie et la participation à la vie sociale, et améliorer la qualité de vie. Les dispositifs d’aide à la communication44 peuvent aussi être utiles aux proches aidants; pour ces derniers, le fardeau a été allégé par le recours à des systèmes de commande oculaire45.
Exercices
La recherche sur l’exercice pour les patients atteints de la SLA n’a pas révélé qu’il était nuisible et selon certaines données probantes, il conférerait un avantage potentiel aux patients aux plans de leur capacité fonctionnelle et de leur qualité de vie46,47. Un programme personnalisé d’exercices, incluant musculation et entraînement aérobique, devrait être préconisé pour les patients qui y sont aptes. Un programme régulier d’étirements et d’amplitude de mouvement est recommandé pour lutter contre la spasticité et la douleur, et prévenir les contractures.
Fonctions cognitives et comportementales
Une dysfonction frontotemporale s’observe chez environ 50 % des patients atteints de SLA3. La dysfonction frontotemporale peut s’accompagner d’une atteinte cognitive ou comportementale qui, chez 20 % des patients, est suffisamment grave pour porter le nom de démence3. Même s’il existe plusieurs outils pour faire le dépistage d’une atteinte cognitive ou comportementale, aucun n’est standardisé. Pour l’instant, il n’existe aucun traitement médicamenteux efficace pour l’atteinte cognitive ou comportementale associée à la SLA. Une approche multidisciplinaire est envisageable pour la prise en charge des comportements particulièrement problématiques.
La présence d’une dysfonction exécutive ou de démence chez les patients atteints de la SLA est associée à une piètre survie48. L’atteinte cognitive ou comportementale ne constitue pas nécessairement une contre-indication à la ventilation non effractive ou à la pose d’une sonde de gastrostomie. Mais avant d’aller de l’avant avec ces interventions chez un patient souffrant d’une atteinte cognitive ou comportementale, il faut toutefois aborder les éventuels problèmes d’observance thérapeutique avec le patient lui-même et ses proches.
Proches aidants
Les soins à la personne atteinte de SLA représentent un lourd fardeau pour les proches aidants. De nombreuses études ont démontré l’incidence de la SLA sur la qualité de vie des proches aidants et les multiples facettes de ce rôle49, mais également la valeur inestimable de la prestation des soins. La progression de l’invalidité50 (score ALSFRS-R) et de l’atteinte cognitive alourdit le fardeau pour les proches aidants51. Les interventions visant à atténuer cette incidence ont été trop peu étudiées pour qu’on puisse formuler des recommandations spécifiques. Les personnes atteintes de SLA sont conscientes du fardeau imposé à leurs proches aidants et elles en souffrent aussi52. Les professionnels de la santé doivent donc être attentifs au bien-être physique et émotionnel des proches aidants, et les faire participer à la planification en vue de l’incidence de la SLA sur le patient et sur eux-mêmes.
Soins palliatifs
Les experts sont en faveur de l’intégration précoce des soins palliatifs pour les patients atteints de SLA8,53. Mais la question des soins palliatifs et des soins de fin de vie est délicate à aborder et n’est pas reçue de la même façon par tous les patients54. Il faut donc tenir compte de l’évolution des besoins et des attentes des patients pour pouvoir amener hâtivement la question des soins palliatifs55. Les experts conseillent à tout le moins d’engager la discussion sur les soins palliatifs si le sujet est amené par les patients ou les proches aidants et s’ils sont indiqués en raison de l’aggravation de la maladie ou de l’invalidité53.
La planification préalable des soins permet au patient de faire connaître ses volontés en la matière avant d’être trop malade et incapable de communiquer. Selon certaines données probantes, il est préférable d’amorcer ces discussions lorsque le patient a accepté que la mort est inéluctable56. Mais les médecins sont souvent réticents à en parler de crainte que ce soit perçu comme une indication que la mort est imminente57. Les outils standardisés pour la planification préalable des soins sont utiles pour mener ces discussions, et non pour donner des directives spécifiques56,58,59. Ces outils peuvent être intégrés dans le suivi de routine de la SLA pour ouvrir la porte à la discussion, en tenant compte de l’état de préparation du patient et de sa façon de prendre des décisions.
Le 17 juin 2016, l’aide médicale à mourir a été légalisée au Canada. Nous avons formulé des recommandations spécifiques sur la façon de répondre aux demandes d’AMM, tant pour aider le patient dans son choix de fin de vie que pour guider les médecins dans cette nouvelle pratique, qui peut soulever une incertitude clinique et de l’inconfort chez certains.
Nous formulons aussi des recommandations sur la possibilité d’effectuer des dons d’organe lors du décès et de la marche à suivre le cas échéant.
Méthodes
Le concept qui sous-tend cette ligne directrice a été développé par la Société canadienne de la SLA avec l’aide de médecins canadiens qui soignent des patients atteints de cette maladie au sein du Réseau canadien de recherche sur la SLA, le Canadian ALS Research Network (CALS), désormais fusionné avec la Société canadienne de la SLA. La ligne directrice a été rédigée à l’aide de l’outil Guideline International Network–McMaster Guideline Development Checklist60, qui explique toutes les étapes de la préparation d’une ligne directrice, notamment la planification, le libellé des recommandations, leur mise en œuvre et leur évaluation. Une description complète de la méthodologie qui a été utilisée est accessible dans la ligne directrice intégrale (www.als.ca/bpr-appendix).
Composition du comité de rédaction des lignes directrices
Un groupe de travail formé de 13 médecins canadiens qui soignent des personnes atteintes de la SLA (les auteurs), présidé par C.S., a dirigé la préparation de cette ligne directrice. Des neurologues et des physiatres actifs au sein du Réseau canadien de recherche sur la SLA qui pouvaient représenter la diversité géographique du Canada ont été invités à participer au groupe de travail. Des médecins qui avaient une expérience dans la rédaction de lignes directrices ont été particulièrement encouragés à participer. Le groupe de travail incluait aussi un gastroentérologue (D.L.) et une pneumologue (A.T.) connaissant bien la SLA. Au début du processus de préparation de la ligne directrice, 2 autres médecins canadiens qui soignent des personnes atteintes de la SLA ont été impliqués, mais ils se sont retirés du projet faute de temps.
Choix des questions clés
En 2014, pour sélectionner les questions cliniques d’intérêt en vue de la rédaction de la ligne directrice, nous avons interrogé les médecins et le personnel des 19 cliniques multidisciplinaires canadiennes de SLA au moyen d’un sondage envoyé par courriel. Le sondage incluait une liste des questions clés utilisées par l’American Academy of Neurology (AAN) et l’European Network for the Cure of ALS lors du choix de leurs paramètres de pratique6,7,8, ainsi que d’autres questions tirées de la propre expérience clinique des membres du groupe de travail. Nous avons demandé aux répondants d’évaluer la pertinence de ces questions en vue de leur inclusion dans la ligne directrice.
Les questions utilisées pour la revue de la littérature sont celles que les participants ont jugées importantes lors du sondage; le groupe de travail les a précisées davantage. Les enjeux cliniques sélectionnés ont été regroupés par thèmes, notamment : annonce du diagnostic, traitement modificateur de la maladie, soins multi-disciplinaires, soins respiratoires, nutrition, traitement des symptômes, atteinte cognitive, risque de thromboembolie veineuse (TEV), exercices, soins palliatifs et soutien aux proches aidants.
Recherche documentaire
En 2015, le Centre for Effective Practice, une firme de consultants experts en rédaction de lignes directrices, a procédé à des interrogations de la littérature sur les questions cliniques sélectionnées dans les bases de données MEDLINE, Embase et CINAHL. Le centre a dégagé les mots-clés pour la recherche sur chacune des questions cliniques en faisant un survol de ceux qui avaient été utilisés pour la ligne directrice de l’AAN6,7 et en consultation avec le groupe de travail. Le centre a procédé à une seconde interrogation de la littérature en décembre 2018 pour recenser des articles publiés après la recherche initiale de 2015. Pour les questions cliniques abordées dans la ligne directrice de l’AAN, les interrogations de la littérature se sont limitées aux publications datant de 2007 à décembre 2018. Pour les nouvelles questions cliniques qui n’avaient pas été abordées dans les lignes directrices de l’AAN et de l’European Network for the Cure of ALS, les interrogations de la littérature se sont limitées aux publications de 1998 à décembre 2018. Les stratégies d’interrogation sont décrites à l’annexe A de la ligne directrice intégrale (www.als.ca/bpr-appendix).
Évaluation de la qualité des données
Le groupe de travail a été scindé par thèmes en plusieurs équipes de 2 membres. Pour les questions relevant d’un thème majeur, 2 membres de chaque groupe ont passé en revue séparément les résumés recensés en fonction des critères d’inclusion et de leur pertinence vis-à-vis de la question clinique. Les critères d’inclusion étaient notamment : lignes directrices publiées sur la SLA et sur la ventilation, essais randomisés et contrôlés (ERC), études cas–témoins, études de cohorte, revues systématiques et méta-analyses. Les publications devaient être en langue anglaise ou française et disponibles en version intégrale. Les rapports de cas, articles de synthèse et publications disponibles uniquement sous forme de résumés ou d’actes de conférence et les thèses non publiées ailleurs ont été exclues. Les publications qui répondaient aux critères d’inclusion selon au moins un des réviseurs ont été entièrement passées en revue par le comité pour une analyse des critères d’inclusion et de la qualité des données et ont reçu une évaluation selon les critères modifiés de l’AAN Clinical Practice Guideline Process Manual (édition 2011) pour classer les études thérapeutiques (encadré no 1). Les tableaux sur les données probantes sont accessibles à l’annexe B de la ligne directrice intégrale (www.als.ca/bpr-appendix).
| Classe | Description |
|---|---|
| I |
|
| II |
|
| III |
|
| IV |
|
* Modifié avec l’autorisation de l’AAN (American Academy of Neurology). 2011. Clinical Practice Guideline Process Manual, Éd. 2011 St. Paul, MN: The American Academy of Neurology. Énoncé de position de l’American Academy of Neurology. Accessible ici : www.aan.com/siteassets/home-page/policy-and-guidelines/guidelines/about-guidelines/11guidelinedevmanual_v408_web.pdf (consulté le 11 septembre 2020).
Élaboration des recommandations
Le groupe de travail s’est réuni régulièrement en personne au moins une fois l’an à Toronto, et lors de téléconférences périodiques pour discuter en détail des énoncés de la ligne directrice. Les comités ont tous rédigé une ébauche de leurs énoncés pour chaque question clinique après avoir tenu compte du libellé des lignes directrices antérieures et des données probantes mises à jour6–8.
Le groupe de travail a passé en revue l’ébauche des énoncés et les a révisés selon une approche itérative, idéalement jusqu’à l’atteinte d’un consensus. En l’absence de consensus au sein du groupe de travail, nous aurions fondé les décisions sur un vote à la majorité des deux tiers (66 %). Toutefois, un consensus a été obtenu pour tous les énoncés, de sorte qu’un tel vote n’a pas eu lieu.
Nous avons attribué à chaque énoncé un niveau de preuve qui incluait le consensus des experts (encadré no 2). Le groupe de travail s’est exprimé nettement en faveur d’inclure des recommandations de pratiques optimales basées sur le consensus des experts en l’absence de données publiées, plutôt que de s’abstenir de toute recommandation. Étant donné le manque de données probantes tirées d’essais cliniques pour orienter les soins dans la SLA, les membres du groupe de travail ont jugé important d’offrir des recommandations pour guider la pratique, plutôt qu’une simple revue des données probantes. Nous avons formulé des énoncés consensuels d’experts basés sur la littérature concernant la SLA ne provenant pas d’essais cliniques, sur les données probantes concernant d’autres maladies ou sur la pratique clinique canadienne actuelle en matière de SLA. Nous avons discuté de l’ordre des énoncés du tableau de recommandations selon leur importance clinique et de la séquence dans laquelle les médecins auraient à les envisager pour leurs patients atteints de SLA.
| Niveau | Type de données probantes |
|---|---|
| A | Au moins 2 études de classe I concordantes |
| B | Au moins 1 étude de classe I ou 2 études de classe II concordantes |
| C | Au moins 1 étude de classe II ou 2 études de classe III concordantes |
| Consensus des experts (CE) | Consensus entre les experts cliniques canadiens de la sclérose latérale amyotrophique en l’absence de données probantes répondant aux critères des niveaux A à C |
* Voir encadré no 1 pour la définition des classes d’études.
Après l’obtention du soutien consensuel du groupe de travail à l’endroit des énoncés concernant les questions respiratoires, la Société canadienne de thoracologie (SCT) a publié une ligne directrice sur la ventilation mécanique à domicile pour les patients atteints de SLA35. Le groupe de travail a trouvé important que nos recommandations concordent avec cette ligne directrice. Nous avons donc comparé chacune des recommandations de la ligne directrice de la SCT à l’ébauche de nos énoncés. Notre groupe de travail a accepté la plupart des recommandations de la SCT sans modifications, si ce n’est certains choix de mots pour plus de cohérence. Nous avons demandé au comité sur la SLA de la SCT de revoir nos suggestions d’énoncés, y compris les énoncés consensuels des experts concernant les questions jugées importantes lors de notre sondage et qui n’étaient pas abordées dans la ligne directrice de la SCT; à la suite des commentaires reçus, des changements mineurs ont été apportés aux énoncés.
Processus de révision
Nous avons préparé un résumé des énoncés de la ligne directrice et le groupe de travail l’a révisé. Lorsque le groupe de travail a été satisfait du libellé des recommandations, y compris du choix de mots, de l’ordre et du classement des données probantes, nous l’avons envoyé aux membres du Réseau canadien de recherche sur la SLA (qui inclut toutes les cliniques multidisciplinaires de SLA au Canada) et à des experts externes (c.-à-d., gastro-entérologie, pneumologie, soins palliatifs et physiatrie) pour leurs commentaires. Nous avons aussi demandé aux cliniques de SLA de soumettre le résumé à leurs équipes multidisciplinaires pour qu’elles le commentent. Le groupe de travail a débattu de tous les commentaires reçus et déterminé quels changements s’imposaient, le cas échéant.
À partir du résumé révisé, une seconde revue externe a été effectuée par des intervenants clés de chaque société provinciale de SLA. Nous avons envoyé par courriel l’ébauche du résumé révisé accompagné d’un sondage comportant des questions ouvertes à chaque section provinciale de la SLA et nous avons demandé à chacune d’interroger ses membres, y compris 1 patient vivant avec la SLA. Tous les commentaires reçus ont été analysés individuellement par le groupe de travail qui y a apporté des modifications à sa discrétion après une discussion approfondie. Les changements consécutifs aux commentaires reçus concernaient surtout les choix de mots. Nous n’avons fait aucun changement substantiel.
Nous avons préparé une version intégrale de la ligne directrice que tous les membres du groupe de travail ont passée en revue pour approbation finale.
Gestion des intérêts concurrents
Tous les membres du groupe de travail ont agi sur une base volontaire et n’ont reçu aucune rémunération pour leur participation. La Société canadienne de la SLA et le Réseau canadien de recherche sur la SLA ont financé l’élaboration de la ligne directrice, y compris les déplacements pour les réunions en personne et la préparation du manuscrit en vue de sa publication.
La Société canadienne de la SLA est une organisation communautaire financée par des donateurs et une partie du financement de ce projet provient de dons amassés lors de l’événement Ice Bucket Challenge. La Société canadienne de la SLA a offert un soutien logistique, mais ne s’est pas prononcée sur le contenu des recommandations. Le Réseau canadien de recherche sur la SLA était un organisme à but non lucratif regroupant des médecins et des chercheurs qui se consacraient à la SLA; mis sur pied pour promouvoir la recherche clinique sur cette maladie au Canada, il était subventionné par des sociétés biotechnologiques qui soumettaient des propositions d’essais cliniques aux cliniques canadiennes de SLA. Le Réseau a par la suite fusionné avec la Société canadienne de la SLA. Même si des membres du Réseau ont participé à l’élaboration de la ligne directrice, le Réseau lui-même n’a joué aucun rôle dans son approbation.
Nous avons discuté de la gestion des intérêts concurrents durant la phase de planification de la ligne directrice; les intérêts concurrents ont été définis comme tout lien pécuniaire avec une société. À l’époque, il n’y avait qu’un seul médicament approuvé par Santé Canada pour le traitement de la SLA : le riluzole. Aucun des membres du groupe de travail ne présentait de conflits d’intérêts en lien avec le riluzole, qui est disponible depuis plus de 20 ans. Nous avons vérifié et confirmé qu’il n’y avait aucun autre conflit d’intérêts potentiel au sein du groupe de travail au début du projet.
En 2017, pendant le processus d’élaboration de la ligne directrice, la US Food and Drug Administration des États-Unis a approuvé l’édaravone pour traiter la SLA. Son fabricant, Mitsubishi Tanabe Pharma, a subventionné des comités consultatifs scientifiques sur l’utilisation de l’édaravone chez des patients atteints de SLA au Canada. En 2018, le médicament a été approuvé par Santé Canada et il a fait son entrée sur le marché canadien en novembre 2019. Certains membres du groupe de travail ont fait partie de comités consultatifs scientifiques de Mitsubishi Tanabe Pharma sur l’édaravone (C.S., M.C., A.I., W.J., C.O., K.S., L Z.); le groupe de travail en a été informé. Tous les membres du groupe de travail ont discuté longuement des énoncés de cette ligne directrice concernant l’édaravone. Pendant le processus de révision de l’ébauche de la ligne directrice, les commentaires des membres du Réseau canadien de recherche sur la SLA et des intervenants clés au sujet des énoncés concernant l’édaravone ont été traités par des membres du groupe de travail qui ne se trouvaient pas en situation de conflits d’intérêts avec Mitsubishi Tanabe Pharma (c.-à-d., n’ayant pas reçus d’honoraires de cette société). Les décisions finales concernant les énoncés sur l’édaravone ont été prises par des membres du groupe de travail qui n’étaient pas en situation potentielle de conflit d’intérêts. Outre l’édaravone, aucune situation potentielle de conflit d’intérêts n’a été soulevée en ce qui concerne les énoncés de cette ligne directrice.
Mise en œuvre
Les recommandations pour les pratiques optimales servent à guider les soins aux patients atteints de SLA au Canada. La ligne directrice sera publiée sur le site Web de la Société canadienne de la SLA (www.als.ca/bpr-appendix). La Société canadienne de la SLA participera aussi à la diffusion de la ligne directrice auprès des membres de la communauté concernée par la SLA, composée de médecins, de membres d’autres professions de la santé, de chercheurs, de patients et de leurs proches aidants, par l’entremise des sections provinciales de la SLA, du Réseau canadien de recherche sur la SLA et des participants au Forum annuel canadien de recherche sur la SLA. Les directeurs de cliniques de SLA et tous les médecins qui soignent des patients atteints de cette maladie seront encouragés à présenter la ligne directrice à leurs équipes cliniques et aux intervenants concernés dans leurs communautés respectives. La Société canadienne de la SLA soutiendra les auteurs de la ligne directrice en produisant des sommaires d’une page sur certains thèmes cliniques clés de la ligne directrice à l’intention des intervenants concernés.
Le groupe de travail appuierait un projet qui étudierait l’incidence de la ligne directrice sur la survie des patients, leur perception de leur qualité de vie et d’autres paramètres spécifiques après sa mise en œuvre comparativement à la période prépublication.
Le groupe de travail s’attend à ce que les données probantes concernant la prise en charge de la SLA évoluent au fil du temps et il prévoit devoir réviser les recommandations tous les 5 ans environ.
Autres lignes directrices
Plusieurs lignes directrices de pratique clinique pour la SLA ont été publiées ailleurs, notamment les paramètres de pratique de l’AAN (2009)6,7, la ligne directrice de la Fédération européenne des sociétés neurologiques sur la prise en charge clinique de la sclérose latérale amyotrophique (2012)8 et la ligne directrice sur l’évaluation et la prise en charge de la maladie des motoneurones élaborée par le National Institute for Health and Care Excellence du Royaume-Uni (2016)9.
L’un des objectifs de la ligne directrice canadienne était de mettre à jour les lignes directrices nord-américaines existantes, spécifiquement les recommandations de 2009 de l’AAN6,7. Comme on l’explique à la rubrique Méthodes, les interrogations de la littérature pour cette ligne directrice canadienne sur les questions cliniques abordées dans les recommandations de 2009 de l’AAN se sont limitées aux nouvelles données probantes seulement (c.-à-d., après 2007), qui ont toutes été classées selon les critères de l’AAN.
Dans la ligne directrice de l’AAN, les recommandations devaient s’appuyer sur des données probantes; ainsi, aucune orientation n’a été fournie en l’absence de données probantes (p. ex., par un consensus d’experts). En revanche, la ligne directrice de la Fédération européenne des sociétés neurologiques a formulé des recommandations à partir du consensus des experts en l’absence de données probantes. Et nous avons décidé de faire de même.
Un autre objectif de la ligne directrice canadienne était d’aborder des enjeux relatifs à la SLA qui étaient absents des autres lignes directrices. La ligne directrice de la Fédération européenne des sociétés neurologiques a ignoré plusieurs enjeux importants pour les patients atteints de SLA au Canada, tels que la gestion de la pharmacothérapie et l’AMM. De même, on ne trouvait rien sur certains enjeux touchant la SLA, tels que les traitements modificateurs de la maladie et l’exercice, dans la ligne directrice du National Institute for Health and Care Excellence.
Comme nous l’avons mentionné précédemment, la SCT a publié une ligne directrice sur la ventilation mécanique à domicile pour les patients atteints de SLA au début de 201935. En collaboration avec la SCT, nous avons veillé à ce que nos recommandations pour les soins respiratoires concordent avec celles de la SCT, mais nous avons ajouté certaines recommandations consensuelles (p. ex., sur la clairance des voies respiratoires).
Connaissances à parfaire
La ligne directrice confirme l’absence de données probantes de grande qualité pour la plupart des aspects de la prise en charge de la SLA; les recommandations formulées se fondent en général sur le consensus des experts du groupe de travail. Il faudra donc approfondir la recherche sur la prise en charge de la SLA, pour élaborer des recommandations fondées sur des données probantes si l’on veut améliorer les normes de soins au Canada et ailleurs. Cette ligne directrice peut orienter la communauté scientifique, ici et à l’étranger, vers les domaines de recherche clinique à prioriser pour la prise en charge de la maladie.
Nous reconnaissons que nous avons été incapables d’aborder tous les aspects de la prise en charge de la SLA dans la présente ligne directrice et que les révisions subséquentes pourraient inclure des aspects qui n’ont pas encore été touchés.
Conclusion
Nous espérons que l’élaboration de la première ligne directrice canadienne sur la SLA sera une importante avancée pour améliorer la vie des patients atteints de la maladie au Canada. Dans cette ligne directrice, la prépondérance des énoncés fondés sur le consensus des experts plutôt que sur des données probantes rappelle non seulement la nécessité d’approfondir la recherche sur la prise en charge de la SLA, mais souligne aussi les défis auxquels les médecins font face lorsqu’ils soignent des patients atteints de cette grave maladie invalidante. Cette ligne directrice permettra aux cliniques de SLA au Canada d’atteindre une norme nationale commune et de s’adapter à mesure que cette norme continuera d’évoluer. Ainsi, les médecins qui soignent des personnes atteintes de la SLA peuvent offrir des soins optimaux à leurs patients et les aider dans leur cheminement les confrontant à cette maladie extrêmement complexe et dévastatrice.
Remerciements
L’équipe de rédaction remercie la Société canadienne de la SLA pour son soutien continu à l’élaboration de cette ligne directrice. Les auteurs remercient aussi Mme Vanessa Blount, qui a aidé à la coordination initiale de la ligne directrice, M. David Taylor et Mme Colleen Doyle pour leur soutien logistique, et Mme Trisha Rao, qui a collaboré à la révision du document. Le Réseau canadien de recherche sur la SLA et des partenaires de la fédération ont aussi formulé des commentaires critiques en ce qui concerne le libellé des recommandations et du manuscrit. Les Drs Ikhlass Salem Haj, Lawrence Korngut et Hannah Briemberg ont eux aussi fourni une aide substantielle à l’élaboration de ces recommandations.
Footnotes
Balados du CMAJ : Entrevue (en anglais) avec les auteurs ici : www.cmaj.ca/lookup/doi/10.1503/cmaj.191721/tab-related-content
Voir la version anglaise de l’article ici : www.cmaj.ca/lookup/doi/10.1503/cmaj.191721
Intérêts concurrents: Christen Shoesmith, Aaron Izenberg, Wendy Johnston, Colleen O’Connell, Kerri Schellenberg et Lorne Zinman ont été membres d’un comité consultatif scientifique sur Radicava (édaravone; Mitsubishi Tanabe Pharma Canada). Christen Shoesmith signale avoir été investigatrice principale d’un site pour plusieurs essais cliniques multicentriques sur la sclérose latérale amyotrophique (SLA). Au cours des 36 derniers mois, la Dre Shoesmith a participé à des essais cliniques commandités par Biogen, Cytokinetics, ALS Pharma et Orphazyme. Marvin Chum signale avoir reçu une bourse de recherche clinique sur la SLA du programme Bernice Ramsay, indépendamment des travaux soumis. Aaron Izenberg signale avoir reçu des honoraires personnels de Biogen, Roche, Alnylam, Genzyme, Takeda et Mitsubishi Tanabe Pharma, indépendamment des travaux soumis. Aucun autre intérêt concurrent n’a été déclaré.
Cet article a été révisé par des pairs.
Collaborateurs: Tous les auteurs ont contribué à l’élaboration et à la conception des travaux ainsi qu’à l’acquisition, à l’analyse et à l’interprétation des données. Tous les auteurs ont participé à la rédaction du manuscrit, en ont révisé de façon critique le contenu intellectuel important, ont donné leur approbation finale pour la version destinée à être publiée, et assument l’entière responsabilité de tous les aspects du travail.
Financement: Le financement pour l’élaboration des recommandations a été fourni par la Société canadienne de la SLA et le Réseau canadien de recherche sur la SLA.